Bronchiolitis Obliterans: Vollständiger Leitfaden – Ursachen, Symptome, Diagnose und Behandlungen
Veröffentlicht am 9. März 2026 von Johann
Angehörige/r einer Person mit BO
Auch bekannt als: Popcorn-Lunge · konstriktive Bronchiolitis · PIBO · BOS · Popcorn Lung
Aktualisiert am 9. März 2026 — Quellen: NCBI, PubMed, Orphanet, ERS/ATS/ISHLT, Frontiers in Pediatrics, RespiRare
Inhaltsverzeichnis
- Zusammenfassung: Was ist Bronchiolitis obliterans?
- Medizinische Definition
- Ursachen und Risikofaktoren
- Pathophysiologie: Was in der Lunge passiert
- Symptome: Wie sich die Krankheit äußert
- Diagnostik: Wie die Krankheit bestätigt wird
- Schweregradeinteilung (BOS nach Transplantation)
- Behandlungen: Aktuelle Therapieoptionen
- Prognose und Verlauf
- Prävention: Wie das Risiko gesenkt werden kann
- Forschungsperspektiven und aktuelle Fortschritte
- Häufig gestellte Fragen (FAQ)
Zusammenfassung: Was ist Bronchiolitis obliterans?
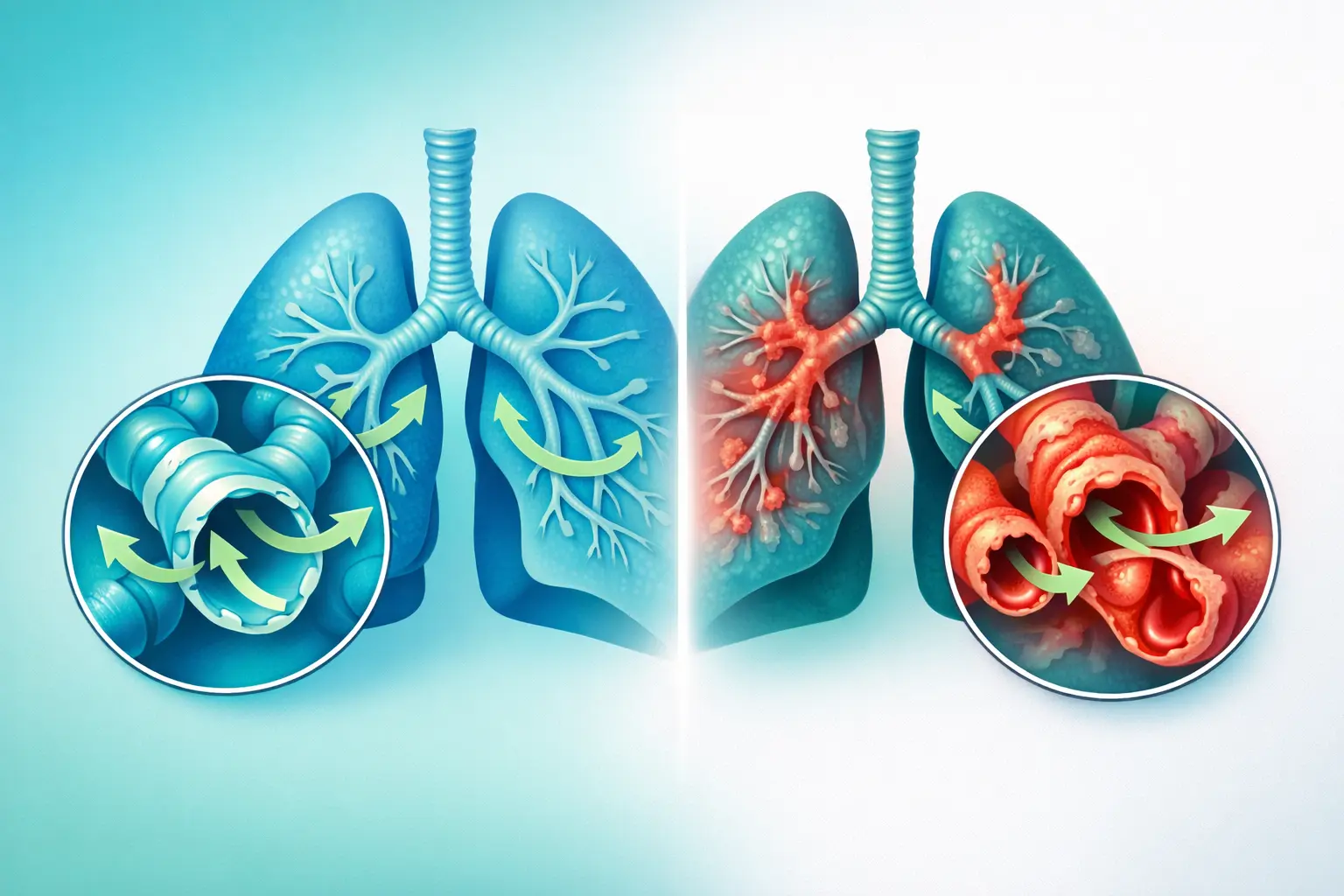
Einfach erklärt: Stellen Sie sich Ihre Lunge wie einen Baum vor. Die großen Äste sind die Bronchien, und ganz am Ende gibt es Tausende winziger Zweige: das sind die Bronchiolen. Die Bronchiolitis obliterans entsteht, wenn diese kleinen Zweige sich entzünden, vernarben und sich fortschreitend verschließen. Die Luft kann immer schlechter zirkulieren. Man atmet schlechter, hustet und ermüdet schnell. Leider sind diese Schäden in den meisten Fällen irreversibel.
Es handelt sich um eine seltene, chronische und schwere Erkrankung. Sie kann sowohl Kinder als auch Erwachsene betreffen, jedoch aus sehr unterschiedlichen Gründen. Bei Kindern tritt sie meist nach einer schweren Atemwegsinfektion auf (man spricht von postinfektiöser Bronchiolitis obliterans). Bei Erwachsenen steht sie häufig im Zusammenhang mit einer Organtransplantation (Lunge oder Knochenmark), dem Einatmen toxischer Substanzen oder bestimmten Autoimmunerkrankungen.
Der Spitzname „Popcorn-Lunge" (oder „Popcorn Lung") stammt aus einer markanten Geschichte: Anfang der 2000er Jahre entwickelten in den USA Arbeiter in Mikrowellen-Popcorn-Fabriken diese Krankheit, nachdem sie jahrelang eine Chemikalie, das Diacetyl, eingeatmet hatten, die dem Popcorn den Buttergeschmack verlieh. Heute wird dieser Zusammenhang auch im Hinblick auf bestimmte Aromen von E-Zigaretten diskutiert, obwohl bisher kein Fall von Bronchiolitis obliterans, der direkt mit dem Dampfen zusammenhängt, bei einzelnen Konsumenten bestätigt wurde.
Anders ausgedrückt: Es handelt sich nicht um die klassische Bronchiolitis des Säuglings (die akut und viral ist), sondern um eine chronische und weitaus schwerwiegendere Lungenerkrankung.
Medizinische Definition der Bronchiolitis obliterans
Die Bronchiolitis obliterans (BO), auch als konstriktive Bronchiolitis oder chronische obliterative Bronchiolitis bezeichnet, ist eine obstruktive Lungenerkrankung, die durch eine transmurale und zirkumferenzielle entzündliche Schädigung der terminalen und respiratorischen Bronchiolen gekennzeichnet ist. Diese Entzündung führt zu einer peribronchiolären Fibrose mit fortschreitendem Verschluss — bis hin zur vollständigen Obliteration — des Lumens der kleinen Atemwege, während die Alveolarräume und das distale Lungenparenchym verschont bleiben.
Die BO ist von Orphanet als seltene Erkrankung klassifiziert (Code ORPHA:1303) und wurde erstmals unter diesem Begriff von Reynaud im Jahr 1835 beschrieben und ab 1981 in der wissenschaftlichen Literatur klar charakterisiert. Ihre genaue Inzidenz in der Allgemeinbevölkerung ist schwer zu ermitteln, aber sie betrifft einen erheblichen Anteil der Transplantierten: etwa 75 % der Lungentransplantatempfänger nach 10 Jahren und zwischen 5 % und 14 % der Empfänger hämatopoetischer Stammzelltransplantationen.
Achtung zur Terminologie: Die Bronchiolitis obliterans (BO) darf nicht mit der Bronchiolitis obliterans mit organisierender Pneumonie (BOOP) verwechselt werden, die heute als kryptogene organisierende Pneumonie (COP) bezeichnet wird. Es handelt sich um zwei klinisch und histologisch unterschiedliche Entitäten. Die BOOP/COP betrifft neben den Bronchiolen auch die Alveolen und spricht in der Regel gut auf Kortikosteroide an, während die BO eine rein bronchioläre Erkrankung ist, die oft therapierefraktär ist.
Ursachen und Risikofaktoren
Die Ursachen der Bronchiolitis obliterans sind vielfältig. Klassisch werden vier große ätiologische Kategorien unterschieden.
1. Postinfektiöse Bronchiolitis obliterans (PIBO)
Dies ist die häufigste Form bei Kindern. Sie tritt nach einer schweren Atemwegsinfektion auf, die das Epithel der Bronchiolen schädigt und eine entzündliche und dann fibrotische Reaktion auslöst, die zur Obstruktion der kleinen Atemwege führt.
Die wichtigsten beteiligten Erreger sind:
- Adenovirus (Serotypen 3, 7, 11, 21 und neuerdings 55) — verantwortlich für 20 bis 69 % der PIBO-Fälle. Bis zu 28 % der Kinder, die eine schwere Adenovirus-Pneumonie überlebt haben, können eine PIBO entwickeln.
- Mycoplasma pneumoniae — zunehmend beteiligt, besonders bei älteren Kindern, mit steigender Inzidenz in Asien.
- Respiratorisches Synzytialvirus (RSV), Influenza, Zytomegalievirus, HIV, HHV-8.
- Bakterielle und fungale Infektionen seltener.
Zu den identifizierten Risikofaktoren für die Entwicklung einer PIBO nach Adenovirus-Pneumonie gehören: Hypoxämie, persistierendes Giemen, Notwendigkeit der mechanischen Beatmung, verlängerte Krankenhausaufenthaltsdauer und Fieberdauer.
Bemerkenswert: Die Diagnose der PIBO wird oft erheblich verzögert. Die Literatur berichtet von einer durchschnittlichen Verzögerung zwischen dem Auftreten der Symptome und der Diagnose von 15 bis 88 Monaten. Diese Verzögerung ist auf die Ähnlichkeit der Symptome mit unkontrolliertem Asthma zurückzuführen.
2. Bronchiolitis-obliterans-Syndrom nach Transplantation (BOS)
Dies ist die Hauptursache für mittel- und langfristiges Versagen der Lungentransplantation. Das BOS gilt als eine Form der chronischen Abstoßung des Transplantats. Mehr als 50 % der Empfänger entwickeln innerhalb von 5 Jahren einen gewissen Grad an BO, mit einer durchschnittlichen Diagnoseverzögerung von 16 bis 20 Monaten.
Nach einer hämatopoetischen Stammzelltransplantation (allogene Knochenmarktransplantation) tritt die BO in 5 bis 14 % der Fälle auf und stellt eine Manifestation der chronischen Graft-versus-Host-Krankheit (GvHD) dar. Das Risiko wird auf etwa 14 % bei Patienten mit chronischer GvHD geschätzt.
Zu den Risikofaktoren gehören: akute zelluläre Abstoßungsepisoden, Vorhandensein von Anti-HLA-Antikörpern, gastroösophagealer Reflux mit Mikroaspirationen, Rauchen und bestimmte virale Infektionen in den ersten 100 Tagen nach der Transplantation.
3. Toxische oder berufsbedingte Bronchiolitis obliterans
Das Einatmen reizender chemischer Substanzen kann eine BO verursachen. Zu den am besten dokumentierten toxischen Agenzien gehören: Diacetyl (Butteraroma), Schwefeldioxid, Stickstoffdioxid (landwirtschaftliche Silos), Ammoniak, Chlor, Thionylchlorid, Methylisocyanat, Flusssäure, Phosgen, Senfgas und Ozon.
Der emblematische Fall des Diacetyls und der „Popcorn-Lunge": Anfang der 2000er Jahre dokumentierte das NIOSH Fälle von BO bei Arbeitern einer Mikrowellen-Popcorn-Fabrik in Missouri, die massiv Diacetyl-Dämpfen ausgesetzt waren. Diese Verbindung (C₄H₆O₂), die natürlich in Butter und Käse vorkommt, verursacht bei massiver und dauerhafter Inhalation eine chronische Entzündung der Bronchiolen.
Der Zusammenhang mit dem Dampfen: 2015 wies eine Studie der Harvard-Universität Diacetyl in einigen aromatisierten E-Liquids nach. 2019 berichtete das Canadian Medical Association Journal über einen Fall bei einem Dampfer. Bisher hat jedoch keine Fallserie formal nachgewiesen, dass Dampfen BO in der Bevölkerung verursacht. In Frankreich und Europa haben die meisten Hersteller Diacetyl aus ihren Produkten entfernt. Vorsicht bleibt dennoch geboten: Mehr als 180 Aromastoffe, die in E-Liquids verwendet werden, wurden nie auf ihre Inhalationssicherheit getestet.
4. Bronchiolitis obliterans bei Autoimmunerkrankungen
Mehrere systemische Erkrankungen sind mit der Entwicklung einer BO assoziiert: rheumatoide Arthritis (am häufigsten), systemischer Lupus erythematodes, entzündliche Darmerkrankungen, Stevens-Johnson-Syndrom, paraneoplastischer Pemphigus und seltener juvenile idiopathische Arthritis oder IgA-Nephropathie.
In seltenen Fällen kann keine Ätiologie identifiziert werden: man spricht dann von idiopathischer oder kryptogener Bronchiolitis obliterans.
Pathophysiologie: Was in der Lunge passiert
Der pathogenetische Mechanismus der BO folgt einem gemeinsamen Schema, unabhängig von der initialen Ursache, wobei bestimmte Besonderheiten je nach Ätiologie variieren.
Phase 1 — Initiale Schädigung: Eine Läsion schädigt die Epithelzellen der terminalen und respiratorischen Bronchiolen. Diese Schädigung kann infektiöser, chemischer, immunologischer oder ischämischer Natur sein. Sie verursacht eine lokalisierte Nekrose des Bronchiolenepithels.
Phase 2 — Dysregulierte Entzündungsreaktion: Die Entzündung der subepitelialen Strukturen führt zu einer Ansammlung von fibrinopurulentem Exsudat im Bronchiolenlumen. Es wird eine Infiltration durch Lymphozyten, Neutrophile und Makrophagen beobachtet. Die proinflammatorischen Zytokine (IL-8, IFN-γ) sind signifikant erhöht.
Phase 3 — Fibroproliferation: Die Entblößung der Mukosa legt die Myofibroblasten der Submukosa frei, die übermäßig proliferieren. Dieser aberrante Reparaturprozess führt zur Ablagerung von Kollagen und sauren Mukopolysacchariden, wodurch das Bronchiolenlumen fortschreitend verengt wird.
Phase 4 — Fibrose und Obliteration: Das Narbengewebe füllt das Lumen der kleinen Atemwege teilweise oder vollständig aus, was zu einer fixen und irreversiblen Obstruktion führt. Manchmal bilden sich intraluminale Polypen (Masson-Körper) durch Proliferation von Histiozyten und Kapillaren.
Im Kontext der Lungentransplantation umfasst der Mechanismus spezifisch eine mikrovaskuläre Insuffizienz und alloimmune Reaktionen gegen das Transplantat.
Histopathologisch werden zwei Typen unterschieden: der konstriktive Typ (peribronchioläre Fibrose mit externer Kompression) und der proliferative Typ (intraluminale Obstruktion durch Granulationsgewebepolypen). Beide Formen können koexistieren.
Symptome: Wie sich die Krankheit äußert
Die Bronchiolitis obliterans ist eine schleichende Erkrankung. Die Symptome sind anfangs oft unspezifisch, was die häufigen diagnostischen Fehler und Verzögerungen erklärt. Sie treten in der Regel 2 bis 8 Wochen nach der initialen Schädigung auf und verschlechtern sich dann fortschreitend.
Die Hauptsymptome umfassen:
- Progressive Dyspnoe: zunächst bei Belastung (Treppensteigen, Laufen), dann in fortgeschrittenen Formen auch in Ruhe. Dies ist oft das erste Zeichen.
- Persistierender trockener Husten: nicht produktiv, der nicht auf klassische Husten- oder Asthmatherapie anspricht.
- Giemen (Atemgeräusche): besonders bei der Ausatmung.
- Chronische Müdigkeit: verminderte Belastungstoleranz.
- Bronchorrhoe: vermehrte Bronchialsekretion in fortgeschrittenen Stadien.
- Späte Hypoxämie: fortschreitende Abnahme der Sauerstoffsättigung im Blut.
Besonders bei Kindern: Die Symptome bestehen über 6 Wochen nach einer schweren akuten Infektion fort, mit Tachypnoe, chronischem feuchtem Husten und diffusen Rasselgeräuschen bei der Auskultation. Das Kind, das zuvor gesund war, erreicht seinen normalen Atemzustand nicht wieder.
⚠️ Achtung — Diagnostische Falle: Die BO wird häufig mit unkontrolliertem Asthma, COPD oder einem einfachen „postinfektiösen Husten" verwechselt. Der entscheidende Unterschied ist, dass die Bronchialobstruktion bei der BO fixiert und nicht reversibel unter Bronchodilatatoren ist, im Gegensatz zum Asthma.
Diagnostik: Wie die Krankheit bestätigt wird
Die Diagnose der Bronchiolitis obliterans basiert auf einer Kombination klinischer, funktioneller und radiologischer Befunde.
Anamnese und klinische Untersuchung
Der Arzt sucht nach einer Expositionsgeschichte (schwere Infektion, kürzliche Transplantation, berufliche Exposition), einer kompatiblen Chronologie und persistierenden, nicht reversiblen Symptomen. Die Auskultation kann exspiratorisches Giemen und/oder Rasselgeräusche zeigen.
Lungenfunktionsprüfung (LuFu)
Die Spirometrie zeigt eine obstruktive Ventilationsstörung, gekennzeichnet durch eine Abnahme des FEV1 (forciertes exspiratorisches Volumen in einer Sekunde), die unter Bronchodilatatoren nicht reversibel ist. Das FEV1/FVC-Verhältnis ist erniedrigt. Der MEF 25-75 kann früh verändert sein.
Hochauflösende Computertomographie (HR-CT)
Dies ist die zentrale bildgebende Untersuchung. Zu den charakteristischen Zeichen gehören: ein sogenanntes „Mosaikmuster" der Perfusion, Air Trapping auf den Exspirationsaufnahmen, Verdickung der Bronchiolenwände und manchmal zentrale Bronchiektasen.
Bronchoskopie und bronchoalveoläre Lavage (BAL)
Die BAL zeigt häufig eine erhöhte Neutrophilie (46 % bis 90 % der Zellen). Sie ermöglicht auch den Ausschluss einer aktiven Infektion.
Lungenbiopsie
Die chirurgische Lungenbiopsie bleibt der „Goldstandard" für die definitive Diagnose. Sie zeigt die peribronchioläre Entzündung, Fibrose und Obliteration des Lumens. Sie ist jedoch invasiv und anfällig für Stichprobenfehler. Die internationalen Leitlinien (ISHLT/ATS/ERS) ermöglichen es nun, die BOS-Diagnose auf Basis des FEV1-Abfalls ohne Biopsie zu stellen.
Weitere Zusatzuntersuchungen
Ein EKG kann Zeichen einer pulmonalen Hypertonie suchen. Die nächtliche Oxymetrie kann Desaturationen aufzeigen. Blutuntersuchungen ermöglichen den Ausschluss anderer Ursachen.
Klinisches Vorhersagetool (Colom & Teper) für PIBO: Ein Score, der auf drei Variablen basiert — typische schwere Bronchiolitis in der Vorgeschichte bei einem zuvor gesunden Kind, dokumentierte Adenovirus-Exposition und Mosaikmuster im HR-CT — ermöglicht eine frühzeitige Verdachtsdiagnose. Ein Score ≥ 7 deutet auf ein hohes PIBO-Risiko hin.
Schweregradeinteilung (BOS nach Transplantation)
Die ISHLT (International Society for Heart and Lung Transplantation) hat Schweregrade definiert, die auf dem prozentualen FEV1-Abfall im Vergleich zum besten Wert nach der Transplantation basieren.
| BOS-Stadium | FEV1 im Vergleich zum besten Wert | Bedeutung |
|---|---|---|
| BOS 0 | > 90 % | Normal |
| BOS 0-p | 81–90 % und/oder MEF25-75 ≤ 75 % | Potenziell (Frühwarnung) |
| BOS 1 | 66–80 % | Leicht |
| BOS 2 | 51–65 % | Mittelschwer |
| BOS 3 | ≤ 50 % | Schwer |
Jedes Stadium wird unterteilt in „a" (ohne histologische Dokumentation) und „b" (mit bioptischer Bestätigung der BO).
Behandlungen: Aktuelle Therapieoptionen
⛔ Wesentliche Information: Die Bronchiolitis obliterans ist eine irreversible und chronische Erkrankung. Es gibt keine kurative Behandlung. Das therapeutische Ziel ist es, das Fortschreiten zu verlangsamen, Symptome zu lindern und Komplikationen vorzubeugen.
Beseitigung der Ursache
Bei beruflicher toxischer Exposition ist die erste Maßnahme das sofortige Beenden der Exposition. Nach Transplantation hat die Optimierung der Immunsuppression Priorität.
Medikamentöse Behandlungen
- Kortikosteroide: systemisch (Prednison, Methylprednisolon) und/oder inhalativ (Fluticason). IV-Methylprednisolon-Stoßtherapien (20-30 mg/kg an 3 aufeinanderfolgenden Tagen, monatlich wiederholt über 3 bis 6 Monate) werden bei Kindern mit PIBO eingesetzt, mit klinischer Verbesserung in der Mehrzahl der Fälle.
- Azithromycin: Makrolid-Antibiotikum mit entzündungshemmenden und immunmodulatorischen Eigenschaften. Standardbehandlung beim BOS nach Transplantation. Prophylaktisch soll es die BOS-Prävalenz reduzieren. Aktuelle Warnungen haben ein potenzielles Risiko einer erhöhten Mortalität durch Tumorrezidiv in bestimmten Kontexten gezeigt, was eine vorsichtige Bewertung erfordert.
- Immunsuppressiva: Cyclophosphamid, Tacrolimus, Ciclosporin — hauptsächlich bei autoimmun bedingten oder posttransplantären Formen eingesetzt.
- Inhalative Bronchodilatatoren: begrenzte Wirksamkeit (fixe Obstruktion), aber teilweise symptomatische Linderung möglich.
- Montelukast: Leukotrien-Antagonist, zunehmend als Adjuvans eingesetzt (FAM-Dreifachtherapie: Fluticason, Azithromycin, Montelukast).
- Zielgerichtete Therapien (Perspektiven): Inhibitoren proinflammatorischer Zytokine sind ein vielversprechender Forschungsansatz.
Nichtmedikamentöse Behandlungen
- Sauerstofftherapie: zu Hause bei chronischer Hypoxämie, insbesondere nachts oder bei Belastung.
- Pulmonale Rehabilitation: strukturierte Übungs- und Schulungsprogramme.
- Extrakorporale Photopherese (ECP): aufkommende Technik bei refraktärem BOS nach Transplantation, ermutigende Ergebnisse.
- Lymphoide Strahlentherapie (experimentell): ermutigende vorläufige Ergebnisse, aber noch niedrige Evidenzstärke.
- Lungentransplantation: letzte Option bei terminalen Formen, einschließlich Retransplantation.
Prognose und Verlauf
Die Prognose hängt stark von der Ätiologie, der Schwere bei Diagnosestellung und dem Ansprechen auf die Behandlung ab.
- PIBO bei Kindern: günstigere Prognose als die posttransplantären Formen. Niedrige Mortalität, aber hohe Chronizität. Etwa 68 % der Kinder haben einen günstigen Verlauf. In seltenen Fällen kann eine teilweise Rückbildung auftreten. Formen im Zusammenhang mit dem Stevens-Johnson-Syndrom sind oft progressiv.
- BOS nach Lungentransplantation: ungünstigere Prognose. Die Wahrscheinlichkeit, nach 5 Jahren BOS-frei zu bleiben, beträgt nur 36 %. Das Überleben nach BOS liegt bei etwa 51 % nach 3 Jahren. Das Sterberisiko ist etwa 6-fach erhöht.
- BO bei Autoimmunerkrankungen: Immunsuppression kann den klinischen Zustand stabilisieren. Variabler Verlauf.
- Toxische BO: stabilisiert sich oft nach Beendigung der Exposition, bildet sich aber in der Regel nicht zurück.
Ohne Behandlung tendiert der natürliche Verlauf zu einer progressiven chronischen Ateminsuffizienz, die tödlich sein kann.
Prävention: Wie das Risiko gesenkt werden kann
- Aktuelle Impfungen: jährliche Grippeimpfung, Pneumokokken-Impfung, RSV-Immunprophylaxe (Palivizumab) für Risiko-Säuglinge.
- Schnelle Behandlung von Atemwegsinfektionen: insbesondere bei Kindern, um bronchioläre Schäden zu begrenzen.
- Atemschutz am Arbeitsplatz: geeignete Ausrüstung bei Exposition gegenüber flüchtigen Chemikalien.
- Rauchentwöhnung und Vermeidung von Passivrauchen: bedeutender verschlechternder Faktor.
- Sorgfältige Überwachung nach Transplantation: regelmäßige Spirometrie und prophylaktische Azithromycin-Behandlung.
- Vorsicht beim Dampfen: zertifizierte E-Liquids ohne Diacetyl oder verdächtige Ersatzstoffe bevorzugen.
- Jeden Infektionskontakt vermeiden: besonders für immungeschwächte oder transplantierte Patienten.
Forschungsperspektiven und aktuelle Fortschritte
Frühe Biomarker: Die Identifizierung biologischer Marker, die eine Diagnose vor Einsetzen der Fibrose ermöglichen, ist eine zentrale Herausforderung. Die Zytokine IL-8 und IFN-γ sowie die Serum-LDH sind in postadenoviralen Formen erhöht und Gegenstand prädiktiver Studien.
Lungenmikrobiom: Studien zum BOS nach Transplantation haben gezeigt, dass mikrobielle Dysbiose mit einem erhöhten BO-Risiko und einem ungünstigeren Verlauf assoziiert ist.
Chinesischer internationaler Konsensus 2023: China hat eine Neuformulierung des Expertenkonsensus zur Diagnose und Behandlung der BO bei Kindern veröffentlicht, die aktuelle Fortschritte in Frühdiagnose und Therapiestrategien integriert.
ERS/EBMT-Roadmap 2025: Eine internationale Arbeitsgruppe hat einen Fahrplan zur Verbesserung der Früherkennung der BO nach allogener Transplantation veröffentlicht, mit Vorschlägen zur Neudefinition der diagnostischen Kriterien.
Prädiktive Modelle und Nomogramme: Klinische Nomogramme ermöglichen die Vorhersage der PIBO-Prognose bei Diagnosestellung, basierend auf der initialen Lungenfunktion und den Zeichen bronchiolärer Entzündung.
Häufig gestellte Fragen (FAQ)
Was ist Bronchiolitis obliterans in einfachen Worten?
Es ist eine Erkrankung, bei der die kleinsten Atemwege der Lunge (die Bronchiolen) sich entzünden, vernarben und sich fortschreitend verschließen. Die Luft zirkuliert immer schlechter, was zu chronischer Atemnot führt. Die Schäden sind leider in den meisten Fällen irreversibel.
Was sind die Hauptursachen?
Die vier großen Ursachen sind: schwere Atemwegsinfektionen (besonders Adenovirus bei Kindern), Organtransplantationen (Lunge, Knochenmark), Einatmen toxischer Substanzen (Diacetyl, industrielle Chemikalien) und bestimmte Autoimmunerkrankungen (rheumatoide Arthritis, Lupus).
Ist Bronchiolitis obliterans heilbar?
Nein, es ist eine irreversible Erkrankung. Die Behandlungen (Kortikosteroide, Azithromycin, Immunsuppressiva, Sauerstofftherapie) zielen darauf ab, das Fortschreiten zu verlangsamen und die Symptome zu lindern. In den schwersten Fällen kann eine Lungentransplantation in Betracht gezogen werden.
Was ist der Zusammenhang zwischen Dampfen und Popcorn-Lunge?
Diacetyl, ein Aroma, das einen Buttergeschmack verleiht, wurde in einigen E-Liquids nachgewiesen. Es ist dafür bekannt, bei Arbeitern, die massiv exponiert waren, BO zu verursachen. Allerdings wurde bisher kein formaler Fall von BO, der direkt durch Dampfen verursacht wurde, im großen Maßstab bestätigt. In Europa haben die meisten Hersteller Diacetyl aus ihren Produkten entfernt.
Was ist der Unterschied zur Bronchiolitis des Säuglings?
Die akute Bronchiolitis des Säuglings ist eine häufige virale Infektion (oft RSV), die in der Regel gutartig ist und innerhalb weniger Wochen abheilt. Die Bronchiolitis obliterans ist eine chronische, seltene und schwere Erkrankung mit dauerhaften Lungenschäden. Es sind trotz ihres ähnlichen Namens zwei sehr unterschiedliche Erkrankungen.
Wie wird Bronchiolitis obliterans diagnostiziert?
Die Diagnose basiert auf der Kombination einer kompatiblen Vorgeschichte, Lungenfunktionsprüfungen, die eine fixe, nicht reversible Obstruktion zeigen, einer hochauflösenden Computertomographie (Mosaikmuster, Air Trapping) und manchmal einer Lungenbiopsie.
Kann man Bronchiolitis obliterans vorbeugen?
Bestimmte Maßnahmen können das Risiko reduzieren: aktuelle Impfungen (Grippe, Pneumokokken, RSV), schnelle Behandlung von Atemwegsinfektionen bei Kindern, beruflicher Atemschutz, Rauchentwöhnung, regelmäßige Überwachung nach Transplantation und Vorsicht mit aromatisierten E-Liquids.
Quellen und Referenzen
- StatPearls / NCBI — Bronchiolitis Obliterans
- Orphanet — Bronchiolitis obliterans (ORPHA:1303)
- ISHLT/ATS/ERS — Diagnosis and Management of BOS (2014)
- RespiRare — Bronchiolite oblitérante non liée à une greffe
- Association Pulmonaire du Québec
- Frontiers in Pediatrics — Risikofaktoren PIBO/Adenovirus (2024)
- Canadian Respiratory Journal — Postinfectious BO in Children (2025)
- Canadian Respiratory Journal — PIBO Workshop Report (2020)
- European Lung Foundation — Behandlung der chronischen pulmonalen GvHD
- National Jewish Health — Bronchiolitis Obliterans
Haftungsausschluss: Dieser Artikel dient ausschließlich zu Informations- und Bildungszwecken. Er ersetzt in keinem Fall eine ärztliche Beratung. Wenn Sie oder Ihr Kind anhaltende Atemsymptome haben, suchen Sie einen Arzt oder Pneumologen auf.